|
|
|||||||||||||
|
当您意识到为了创造宇宙而被设计的自然法则如此超乎绝伦时, 您会发现,宇宙绝对不是偶然出现的, 它的背後肯定存在着一个目的° .........................英国物理学家-约翰.泊金鸿84 到目前为止, 我们已研究了所有生命必需的物理平衡° 我们瞭解到宇宙的总體结構, 地球在宇宙裏的位置, 地球的物理特徵, 空氣、光线和水都是按照生命必需的方式得到特别设计的° 除此之外, 我们还应研究構成我们身體的基本元素的成份° 我们的手、眼睛、头发、肺和肝脏或者给我们提供营养的所有动物、植物、树木、禽类的组成元素都是经过特别设计的° 正如物理学家E.D.克拉克所说的那样, “造物主为了营造生命而製作了特殊的零件°” 85. 真主赋予了所有生命非常特殊和超乎绝伦的構造° 这些構造的最基本元素是碳原子° 碳的设计
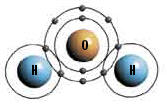
正如我们在以前的章节裏所说过的那样, 碳在化学元素週期表裏排在第六位, 並瞭解了它在红色巨星裏的製作过程° 发现碳的绝妙構成经过的霍伊尔说过, “如果我们注意星體裏发生的结果的话, 我们不难看到, 物理原理都是有意识地得到安排的°” 86 在研究碳的结構时, 我们会发现, 不仅碳原子的结構, 而且它的化学特徵也是有意识地被创造的° 在自然界, 纯碳有两種形式:石墨或者宝石° 由於不同的组合, 出现了许多不同的物质, 例如, 细胞膜、树皮、视網膜、鹿角、蛋黄、蛇毒等都是由碳構成的° 碳和氢、氧核臭氧原子分别合成後, 構成了不同的物质° 有些碳化合物只有幾个原子構成, 有些则由上千, 甚至上百萬个原子構成° 只有碳原子才能構成这種寿命长的结構° 戴维.波尼在其题为《生活》的书裏指出, “碳是超乎寻常的元素.假如碳没有这些特殊特徵的话, 世界上的生命是不会出现的°” 87 英国化学家奈维尔.斯德维克, 在其名为‘化学元素和它们的结構’的著作裏是这样描述碳原子的: “在構成化合物和種类方面, 碳不同於任何元素° 到目前为止, 已发现的碳化合物有50萬種° 即便这样, 这还不足於我们认识碳, 因为碳是组成所有物质的基本元素°” 88 没有任何元素能够取代碳的位置° 曾被认为能够代替碳的矽, 也被证明无法勝任这个工作° 斯德维克说, “我们已有足够的证據认为, 矽无法替代碳来充当生命的基本元素°” 89 共價键 当碳和其他原子合成有機物时, 原子之间的链被称为‘共價键’° 电子在原子核周围的轨道上旋转° 在離原子核最近的轨道裏只能有两个电子° 在第二个轨道裏有18个电子, 以次类推°有趣的是, 原子都趋向於完成轨道裏的电子数量° 例如, 在第二个轨道周围裏有6个电子的氧原子会努力往其轨道裏在增加两个电子, 其中的原因无人能够知晓° 不过, 假如没有这个倾向的话, 会不会出现有機物的° 共價键正是这種倾向的需求下成立的° 两个具有这種倾向的原子会通过电子完成这个步骤° 例如, 组成水的两个氢原子和一个氧原子会建立共價键° 氢原子的第二个轨道的电子从而增加到8个, 氢原子的电子数也增加到两个° 碳正是通过这種共價键合成了许多不同的物质° 甲烷便是其中之一° 甲烷是由四个氢原子通过共價键和碳合成的° 碳的原子数(6个)比氧的原子数(8个)少两个, 所以, 碳和氢建立了共價键°
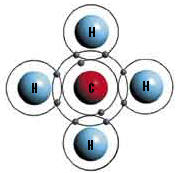
不过, 正如前面所说过的那样, 碳建立的共價键的範围很广° 碳仅和氢建立的‘碳氢化合物’的種类就很多, 包括天然氣、液化油、汽油、柴油和多種機油° 被称为乙烯和丙稀的碳氢化合物是石油化工的基石° 其他的碳氢化合物有苯、甲苯和松脂等° 在櫃子裏对衣服起保护作用的卫生球是另外一種碳氢化合物° 由氯和氟合成的碳氢化合物有麻醉剂、灭火剂和氟利昂等° 碳, 氢和氧通过共價键形成另外很多種有機物° 它们其中有乙烷和丙烷之类的酒类, 还有乙醛, 和脂肪酸° 由碳, 氢, 氧構成的第二类物甲烷氣體的结構:位於中间的碳原子和周围的四个不同的氢原子相连° 碳, 氢, 氧和氮利用共價键还会形成非常重要的结構, 这種最基本的结構就是脱氧核糖核酸(DNA)° 组成DNA的原子还是碳, 氢, 氧和氮° 总之, 碳的共價键是使生命存在的必要条件之一° 如果我们不能用共價键将碳, 氢, 氧和氮组合在一起, 那麼我们无从谈起生物的生存° 碳之所以有这種结合形式是因为有化学上称之为“亚状态” 的属性° 著名化学家J.B.S.哈裏当那, 对这一属性有这段解释: 一个分子有亚稳态, 意味着在一定的範围之内, 它可释放和吸收能量, 但在光, 射线, 和催化剂的作用下却是非常稳定的°90°
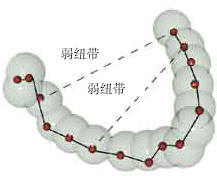
这種技术解释是指炭原子可以很多形式结合成为分子°碳原子可和许多原子以共價键结合成为分子°但是我们有必要提起到° 碳原子的亚稳态只有在很小的一个温度範围之内是有效的° 如果超过100度, 碳原子就没有任何规律可言° 这在日常生活中我们经常遇到° 当我们烹饪肉时, 实际上我们在改变它的结構° 但是我们需要对一些地方进行特别的注意: 让烹饪的肉处於真正的“死” 的状态, 也就是改变肉的结構° 大部分碳水化合物在高於100度时会发生分解° 维他命(维生素)也会立刻分解° 糖也会分解, 营养成份会降低° 如果到达150度, 那麼碳就会聚积在一起, 然後开始燃烧° 换句话说就是, 共價键的形成是不能超过100度的, 同时也不能低於零度° 零度以下对生命活动是不可能的° 但是其他化合物不是这样的, 即使在很高的温度下, 它也不会分解° 我们可以做这样一个试验, 我们在两个锅裏分别放上肉和石头, 在一定温度以上肉的形状和结構就发生了变化, 而石头却没有任何变化° 如果我们将温度再提高一些, 石头也不会发生任何变化° 如果您注意的话, 共價键的形成和分解的温度範围正好和地球的温度範围一致° 就像我们在前面提到的, 在宇宙中, 温度有从上萬的星球到接近绝对温度的-273.15度° 而我们人类生活的地球正好有碳形成化合物所需的条件, 这正说明瞭地球是特别的, 是为生命生存设计的° 光的另一个有趣的特点是, 它给地球的温度正好使水处於液态° 並且水处的液體的温度與碳與其他物质合成所需的温度正好相等° 这样一个条件是很难在其他的星球上发现的° 水,碳以及地球的很多属性, 它们之间一一配合, 从这一点可看出地球是特别为人类创造出的° 弱纽带 把人體的所有原子凝聚在一起的不是共價键, 而是被称为‘弱纽带’的第二类键° 弱纽带的力量比共價键小差不多20.倍° 尽管如此, 在有機化学裏却有着極重要的地位° 身體的基石蛋白质正是在弱纽带的连接下才获得三维形状的°蛋白质一般被称为‘氨基酸链’° 不过, 这種定义还不够完整° 因为‘氨基酸链’这个名称会使人想到一个链条上串在一起的珍珠° 组成蛋白质的氨基酸链如不同的树枝上的树叶那样具有三维機構° 共價键把構成氨基酸的原子凝聚在一起, 弱纽带则给它们赋予了三维形状° 在一个蛋白质不存在的环境裏生命是不会存在的° 有趣的是, 弱纽带所需的温差和共價键的相同, 尽管弱纽带和共價键和结構完全不同° 没有任何自然原因可以说明弱纽带和共價键需要相同的温差° 假如它们所需的温差不同的话, 那麼, 蛋白质的生产是不可能发生的° 我们发现和碳原子超乎绝伦的特徵有关的所有这些知识说明, 生命的基本因數原子, 水和地球之间存在着绝对的和谐° 麦克尔.丹顿在其名为《自然的归宿》的书裏强调这个事实时, 这样说道:
“在宇宙裏温度圈裏有一个独一无二的温度间距, 在这个间距裏我们拥有. (1)水, (2)处於亚稳态的多種多样的有機合成物, (3). 给複杂的分子機構思念未形状的弱纽带°” 91 正如我们在前面提到的那样, 在宇宙裏只有地球才拥有这个狭窄的温度间距° 生命的两个重要支柱碳和水, 在地球上的数量極多° 所有这些无不说明, 碳原子和它超乎绝伦的構造是为了人类的生存得到特别设计的° 地球则是为了使一个以碳为基础的生活成为可能而得到特殊设计的°
氧氣的设计 刚才我们说过碳是生命的最基础元素, 是经过特别设计的° 能量是所有生命得以生存的第二个条件° 绿色植物从太阳获取能量° 而动物和人的能量经过氧化,即‘燃烧’拉获取能量° 我们通过燃烧从植物获取的营养来得到能量° 氧化是指和氧氣发生反应° 由於这个原因, 氧氣如水、碳一样是生命的基本条件之一° 给我们能量的‘燃烧’过程的公式如下:碳化合物+氧氣>水+二氧化碳+能量 经过上述反应, 在水和二氧化碳旁边会有大量能量出现°碳化合物中最重要的是碳氢化合物° 例如葡萄糖便是给人體提供能量的基本的碳氢化合物之一° 構成碳氢化合物的碳原子和氢原子是最容易氧化的原子°氢原子是所有原子中发生氧化反应时释放能量最高的原子° 换言之, 氢原子是氧氣的最好的‘燃料’° 从‘燃烧價值’来讲, 碳原子在氢原子和硼原子之後, 名列第三位° 在《环境的適宜性》这本书裏, 罕德森对这種‘超乎绝伦的和谐’表示驚讶不已, 写道: “从生理学带来最佳结果的化学反应也是给生命带来最佳能量的反应°” 92
火的设计(我们为何不一下子燃烧起来?)
的確是个令人驚讶的事情° 之所以这样是因为氧氣在正常状态下的O2分子的大半不参加反应° 那麼, 这个不容易参加反应的分子在人體裏是如何发生反应的呢?从19世纪以来被人们争论的问题, 在近50年来的科学研究中终於有了答案° 生化试验结果表明, 人體裏的某些特殊酶让只在大氣中存在的O2分子发生反应° 这些特殊酶在複杂的工序之後, 把人體内的铁和铜当作催化剂来使用, 从而使氧氣产生活性°93 在这裏有一个很有意思的局面:氧氣是个易燃元素, 应该使人體燃烧° 为了阻止这个局面, 大氣中的氧氣-O2分子‘失去’活性, 也就是不轻易发生反应° 然而, 人體为了获得能量必需利用氧氣的燃烧特性° 正是由於这个原因, 在人體细胞被赋予了啟動O2分子的酶系统°在这裏值得一提的是这種酶系统是那些用偶然来解释一切的进化论者无法解释的一種设计°94 另外一个阻止人體燃烧的措施是被英国化学家那维尔.斯德维克称为‘碳特有的不燃性’95° 也就是说, 碳原子在正常的温度裏, 是不容易和氧氣发生反应的° 在现实生活中, 我们常经历一些寻常现象, 如在冷天裏木材或者煤炭不容易点着, 这是碳的特有的‘不燃性’在作怪° 但是一旦火点着後碳会立刻发生反应, 释放出巨大的能量° 由於这个原因, 如果不用火柴或者其他易燃品, 火灾是不容易发生的°从上述的情形来看, 火是个特殊设计的结果° 氧氣和碳的被设计的化学特徵决定了它们在高温下才会燃烧° 假如不是这样, 世界上的生命是不会存在的° 如果氧氣和碳燃烧的倾向在强一点的话,氣温升高一点, 人體、树木和动物会立即起获燃烧的° 假如一个在沙漠裏跋涉的人在氣温升到最高的时, 在这種前提下, 他的身體会起火燃烧° 植物和其他动物也会面临同样的危险° 当然, 在这世界裏, 人类是不可能生存的° 同样, 氧和碳的‘不燃性’在一点的话, 那麼, 在世界点火就会变得很难, 甚至於不可能° 在火不存在的一个环境裏, 人类无法取暖, 科学也不会进步, 因为科学是建立在金属之上的° 金属只在高温下才会变软, 成形°麦克尔.丹顿是这样描述氧氣和碳对生命之重要性的: “碳和氧原子在正常的温度裏不发生反应的倾向和一旦发生反应释放出巨大能量这些特性, 是为了世界上的生命而得到的特殊设计° 正是因为碳和氧原子有这種特殊的设计, 複杂生物的控制和有秩序的获取能量及人类利用得到控制的火获取了发展科学所需的温度才成为可能°” 96 换言之, 碳和氧是为了我们的生存而得到特别设计的° 这两種元素的特性使得我们有了点火和並適当使用它的機会° 地球上的许多地方都布满了供我们燃烧用的树木° 这表面, 火及火材是为了人类的生存而得到最佳设计的° 真主在古兰经裏是这样给人类启示的: “他为你们用绿树创造火, 你们便用那绿树燃火°” (雅辛.章, 第80节) 氧氣的理想融解 人體之所以能使用氧氣是因为其在水裏可以溶解° 在我们呼吸时进入肺裏的氧氣会立即融入血液裏° 血液裏的血红蛋白会把已融解的氧氣分子撲捉後运到细胞裏° 如我们刚才所描述的那样, 在酶系统的作用下, 在细胞裏三磷酸腺苷会被氧化,然後获取能量° 所有的複杂生命都通过这个工序获得能量° 当然, 这个系统只有在氧氣能够溶解的前提下才能工作° 假如氧氣溶解性差一点的话, 那麼, 进入血液的氧氣数量不会多, 从而不足於满足细胞获取能量° 假如氧氣的溶解性强一点的话, 那麼, 血液裏的氧氣量会剧增, 从而会发生‘氧氣中毒’事件° 有趣的是, 不同的氣體在水裏的溶解度相差一百萬倍, 也就是最易溶解和最难溶解的氣體之间差别是一百萬倍° 幾乎没有一个氣體的溶解度是相同的° 例如, 二氧化碳比氧氣的溶解度要高20倍° 不过, 氧氣的溶解度正好符合人类所需的标准° 假如氧氣的溶解度差一点或者强一点会怎样呢? 假如氧氣溶解都差一点的话, 那麼, 进入血液的氧氣数量不会多, 从而不足於满足细胞吸收氧氣的需要° 在这種情况下, 像人类这样的高级动物会难以生存° 无论您怎样增加呼吸次数, 都是无济於事的, 因为空氣裏的氧氣进入细胞的数量不够, 因此, 人会面临逐渐窒息的危险° 假如氧氣溶解都强一点的话, 那麼, 进入血液的氧氣数量会太多, 从而会发生‘氧氣中毒’现象° 氧氣实际上是个很危险的氣體, 在量超过正常水平的时候是会致命的° 过多的氧氣进入血液的话, 会产生具有毁灭力的副产品° 人體裏具有能够避免这種局面的酶系统° 不过, 在氧氣量过大的时候, 酶系统也不会发挥作用, 人会逐渐中毒而死去° 化学家埃尔文.弗裏德维奇说: “靠呼吸生存的有機體落入了一个有趣的陷阱裏° 维持它们生命的氧氣與此同时也具备毒性° 这種危险在设计绝妙的防禦系统下得到避免°” 97使我们免於掉入这个陷阱, 即窒息或者氧氣中毒危险的东西是氧氣恰到好处的溶解度和酶系统功能° 更明確的说, 真主给我们製造了超乎绝伦的空氣和使用这个空氣的系统° 其他因素 很显然, 为人类的生存而特别设计的因素不局限於碳和氧° 在人體内也占较大比例的氢和氮对人类的生存也是極为重要的° 除此之外, 在化学元素週期表裏的所有元素以各種形式被赋予了维持生命的作用° 在週期表裏, 从氢到铀有92个元素(铀元素之後的元素在自然界是不存在, 在试验室裏製成的元素都不稳定)° 这92个元素裏的25个对生命的存在有直接的关系° 它们中的11个, 即氢、碳、氧、氮、钠、镁、磷、硫、氯、钾和钙是组成生命99%的成份° 它们之外的其他14个元素, 即钒、铬、锰、钴、铁、镍、铜、锌、钼、硼、矽、铯、氟和碘在生物體内占很小的比例° 但是它们的作用是很大的° 另外°像铝、砷和钨也在某些有機合成中发挥作用, 去解决没有完全溶解的部分° 溴、钡和锶这三个元素在更活跃的有機合成中发挥作用, 不过它们的工序尚未被搞清楚°98 这个範围包括了元素週期表裏的各種原子° 从而, 这个週期表裏的所有元素为生命的维持在各司其职° J.J.R.福乐索.德席尔瓦和R.J.P.威廉斯在他们所著的《元素的生物化学》一书裏, 这样写道: “生物元素是从週期表裏的各種元素和次元素裏得到特别选择的, 这使得各種化学特性根據环境要求和生命工序保持着联系°” 99 在週期表裏排在最後的放射性元素也对生命的维持有一定的作用° 麦克尔.丹顿在其《自然的归宿》一书裏所描述的那样, 放射性元素裏的铀, 在地球的地质形成上发挥了重要作用° 地核裏的温度是在放射元素的作用下得到储藏, 因此在地核裏有液态铁的积累, 从而使地球的磁场得到了保护° 在週期表裏看上去对生命的维持没有太大作用的元氣和稀有金属则在原子製造上的必经之路°100 总之, 我们所知道的宇宙裏的元素对生命的维持发挥着作用° 没有任何一个元素是无缘无故出现的° 这是宇宙由真主创造的另外一个证據° 结论 经过研究, 我们发现, 宇宙的物理和化学特性都正好符合生存 的标准° 无论这種研究深入到什麼层次, 这个道理是不会变的° 在宇宙的每一个部分都显示了一个目的及和这个目的有关的完美的和谐、设计和平衡° 很显然, 这種局面表明, 存在着一个创造了宇宙的崇高的造物主° 无论我们如何研究物质的特性, 我们都会意识到让宇宙从无到有的真主之无上的知识、智慧和萬能° 所有的东西都聽命於他, 因此所有的一切都在和谐之中° 20世纪科学发展得出的结论印证了古兰经裏的启示° 真主在古兰经裏是这样降下关於他无上的创造艺术的: “多富哉拥有主权者!他对於萬事是全能的° 他曾创造了生死, 以便他考验你们谁的作为是最優美的° 他是萬能的,是至赦的° 他创造了七层天, 你在至仁主的所造物中, 不能看出一点参差° 你在看看!你究竟能看出什麼缺陷呢?然後你在看两次, 你的眼睛将昏花地、疲倦地转回来!” (姆勒克..章, 第1节至第4节) |
| ||||||||||||
| | |||||||||||||
| | |||||||||||||
| | |||||||||||||
| |